イベルメクチンによる河川盲目症の撲滅
- 山梨の目医者
- 2021年2月11日
感染症の原因である病原体には細菌、真菌、ウィルス、寄生虫などが含まれます。
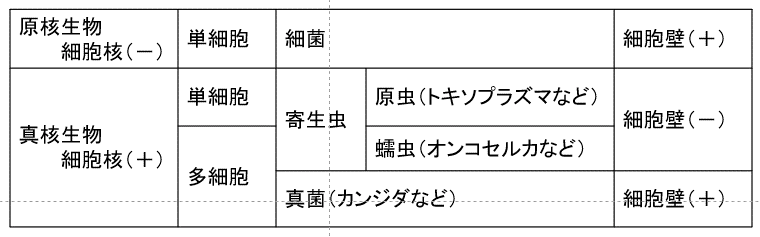
一方、生物は細胞核の有無によって原核生物と真核生物に分類されますが、細菌は原核生物であり、真菌と寄生虫は真核生物です(ウィルスは細胞をもたず、自己複製能がないので生物とはみなされません)。
抗菌薬
細菌の治療に用いられる抗菌薬はヒトには安全で細菌のみを障害しますが、それは細菌とヒトの細胞構造の違いによります。
たとえばペニシリンなどβラクタム系薬剤は細菌の細胞にある細胞壁の合成を阻害しますが、ヒトの細胞には細胞壁がないので大きな障害はありません。
マクロライド系あるいはアミノグリコシド系の抗菌薬は蛋白合成に必要なリボソームのうち、原核生物に特有の沈降係数70Sのリボソームを障害しますが80Sの真核生物には作用しません。
寄生虫治療薬イベルメクチンの作用
しかし寄生虫は同じ真核生物であるヒト細胞と異なる点が少ないため、その治療薬の開発は困難でした。
しかしノーベル賞を受賞した大村智先生らが発見したイベルメクチンが、蠕虫に分類されるオンコセルカ(回旋糸状虫)に効くことがわかりました。
イベルメクチンは無脊椎動物の神経や筋の細胞膜にある塩素イオンチャンネルを開いて細胞外の塩素イオンを流入させ、細胞の過分極による麻痺で死滅させます。
一方、ヒト細胞の塩素イオンチャンネルへの結合は弱いので副作用はわずかです。
http://www.antibiotics.or.jp/MLs/12th/12th_MLs_106.pdf
オンコセルカ症の眼症状
オンコセルカ症は流れの速い河川にのみ生息するブユ(中間宿主)がヒト(終宿主)を吸血することで感染が蔓延する熱帯地方の病気ですhttps://meisha.info/archives/1028。
オンコセルコーマと呼ばれる皮下の腫瘤内に寄生している雌の成虫は、体長0.2-0.4mmのミクロフィラリアを1年に最大百万匹産みます。
ミクロフィラリアはヒトの体内では成虫になることができない幼虫で、成虫になるにはブユ体内に取り込まれて感染幼虫になることが必要です。
ミクロフィラリアの多くは皮下(組織学的には真皮上層)に存在しますが、好んで眼球内にも侵入します。
生きているミクロフィラリアによる害は目立ちませんが、死滅する時に硬化性角膜炎sclerosing keratitis、虹彩炎、視神経炎、網脈絡膜炎など種々の眼炎症を生じて失明に至ることがあります。
感染して失明する患者がブユの生息地である河川流域に多く見られるので河川盲目症と呼ばれます。
Onchosercariasis. In: Albert DM, Jakobiec FA, eds. Principles and practice of ophthalmology 2nd edition. Philadelphia: WB Saunders. 4922-4. 2000
オンコセルカ症撲滅計画
感染者がイベルメクチンを内服すると48時間で皮下に存在するミクロフィラリアは死滅します。
成虫は死にませんが、その子宮内のミクロフィラリアは死滅するため、ミクロフィラリアの新たな供給がストップします。
ブユが吸血しても皮下のミクロフィラリアは消失しているので、感染の拡がりを阻止します。
成虫は14-15年生きますが1987年からスタートしたいくつかの国際的な撲滅プログラムでの、毎年1-2回の集団投与戦略でオンコセルカ症は撲滅されようとしています。
https://www.forth.go.jp/moreinfo/topics/2017/02011141.html
余談
オンコセルカ症撲滅計画で使われるイベルメクチンはメルク社から無償供与される薬剤でメクチザンと呼ばれます。
日本でも手に入る医療用医薬品のイベルメクチンはストロメクトールと呼ばれ、疥癬(ヒゼンダニの寄生による皮膚の病気)と腸管糞線虫症に適応があります。
詳細な機序は不明ですが、新型コロナウイルス感染症(COVID-19)に効果があるとする報告があり、臨床治験もされているようです。https://plaza.umin.ac.jp/aga/covid19/stromectol.html


